Importancia de biopsiar un tumor
Una biopsia es un procedimiento que se realiza para extraer una pequeña muestra de tejido el cuerpo para su análisis en un laboratorio
Es importante llevar a cabo una biopsia para saber qué tumor tenemos y a qué subtipo pertenece. No todos los tumores son iguales y no todos los tipos de cáncer de mama se tratan igual. La biopsia nos permite hacer un análisis genético, es decir, averiguar qué características o mutaciones en concreto tiene ese tumor. Esto es lo que permitirá determinar el tratamiento específico.
Como algunos tumores van cambiando con el tiempo, en parte por los diferentes tratamientos que se van administrando, las biopsias permitirán conocer su evolución.
Actualmente hay dos opciones de biopsia: la de tejido y la líquida.
La biopsia de tejido es la tradicional. Aunque nos proporciona información del tumor y las características moleculares, es una técnica invasiva que en ocasiones no es fácil de llevar a cabo. A veces la aguja no llega a pinchar bien la lesión por su localización. Además, hay algunos riesgos, aunque poco frecuentes, como son la posibilidad de sangrado o la producción de dolor, que complican la técnica y dificultan su repetición.
En cuanto a la información, la biopsia de tejido no recoge la heterogeneidad tumoral. Por ejemplo, no todas las lesiones metastásicas de un paciente son iguales. Podemos tener una lesión en el pulmón y otra en el hígado, y si hacemos únicamente una biopsia del pulmón solo tendremos la información de ésta. El problema de la heterogeneidad se puede subsanar con la biopsia liquida.
¿Qué es la biopsia líquida?
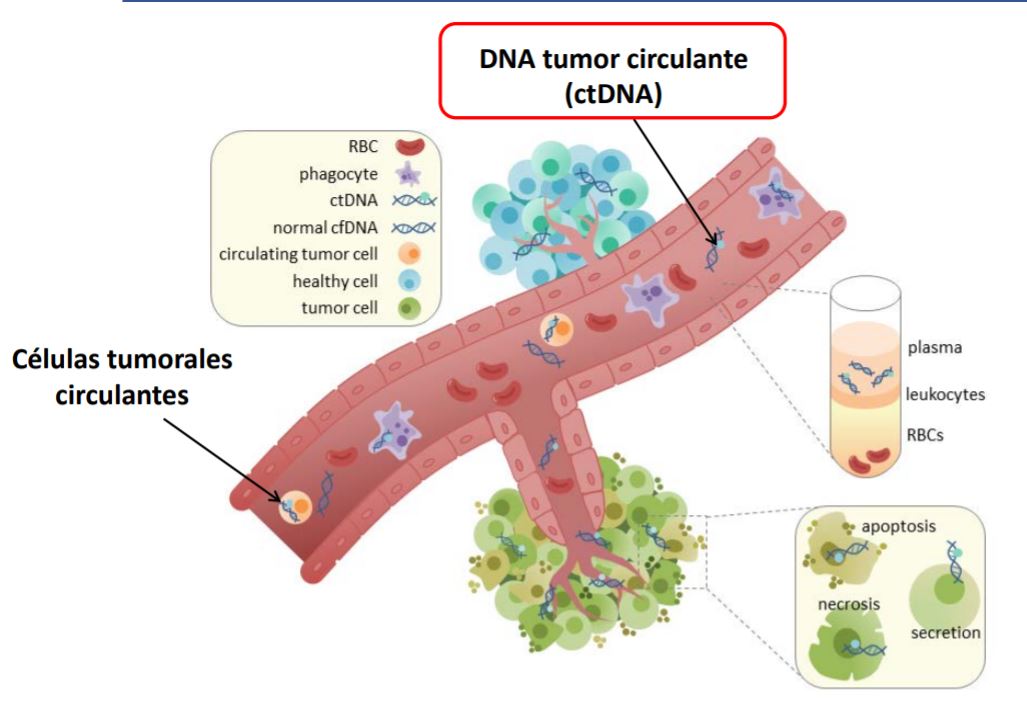
El tumor puede liberar células tumorales en la sangre. Éstas pueden morir o bien desprender trocitos de material genético, al que llamamos ADN tumoral circulante (siglas en inglés ctDNA). Estos trocitos se encontrarían en el plasma, separados de otras células de la sangre como los glóbulos rojos y los blancos.
Este ctDNA tiene una vida media muy corta, es decir, cuando se libera esta materia en la sangre, rápidamente se irá eliminando por el riñón o por el hígado, de manera que dura unas dos horas en la sangre. Por lo tanto, una extracción de sangre después de la cirugía podría ser un mejor predictor de la recurrencia de la enfermedad que la medición inicial (1).
El National Cancer Institute de Estados Unidos, define la biopsia líquida como una prueba que se realiza en una muestra de sangre para buscar células cancerosas de un tumor que circulan en la sangre o fragmentos de ADN de células tumorales que se encuentran en la sangre (2). Es decir, consiste en el análisis molecular a través de extracciones de sangre, aunque también se pueden analizar en otros líquidos del organismo como son el que recubre las meninges, el que recubre el pulmón, la saliva o incluso la orina. El concepto de biopsia liquida es muy amplio, pero habitualmente se habla de la analítica de sangre. A diferencia de la biopsia de tejido, permite realizar el análisis molecular, pero de una forma mucho más sencilla y rápida. Podemos hacer una analítica de sangre en cualquier momento, y además la podemos ir repitiendo para monitorizar el tumor.
Lo que se pretende identificar en las muestras son las diferentes mutaciones propias del tumor, ya que estas mutaciones no están presentes en el resto de células normales que hay en la sangre. Las técnicas utilizadas son muy sensibles, y por muy poca cantidad de ADN tumoral que exista en la sangre o en otros líquidos, se podrá detectar y analizar.
Si se hace este análisis con alta frecuencia, se va construyendo una película de la evolución de la enfermedad, añadiendo lo que está sucediendo en el momento actual de cada extracción. Los marcadores tumorales, sin embargo, no proporcionan un reflejo tan instantáneo de lo que está ocurriendo en la enfermedad, ya que a veces informan de lo que estaba sucediendo incluso algunos meses atrás.
Utilidades y aplicabilidad
En los últimos años se ha progresado mucho en esta técnica, sobre todo en cáncer de pulmón y colorrectal. Ahora también se está avanzando en el de mama y próstata.
Gráfica 1.Utilidades biopsia líquida. Xemio en Colaboración con SOLTI.

Como se indica en la Gráfica 1. esta técnica es útil en el seguimiento de la enfermedad. Actualmente, está técnica todavía está en desarrollo y no se aplica en la práctica habitual
El seguimiento potencial que ofrecería esta técnica se podría dar en diferentes etapas de la enfermedad y hay múltiples investigaciones en marcha para validarlo:
- La enfermedad localizada. En ocasiones el tumor se encuentra en la mama, es muy pequeño y ni siquiera se palpa. Con esta técnica podríamos detectar hipotéticamente esta alteración en la sangre y adelantarnos al diagnóstico clínico, mucho antes de que la paciente se lo palpe o sea visible en la mamografía.
- Cuando el tumor ya se ha diagnosticado y se ha operado. La biopsia líquida permitiría hacer el seguimiento de la enfermedad. Tras la extirpación del tumor el porcentaje de ADN tumoral en la sangre debería caer a cero. Si por el contrario queda algo de éste en la sangre, podremos sospechar que queda enfermedad residual.
- Durante los años siguientes a la operación, la biopsia líquida permitiría hacer el seguimiento. Si volviera a aparecer el ADN tumoral en la sangre, podríamos estar ante una recidiva y se podría detectar el tumor antes de que lo fuera a la palpación o visible en las pruebas de imagen. Hipotéticamente, serviría para hacer un diagnóstico precoz de la recaída.
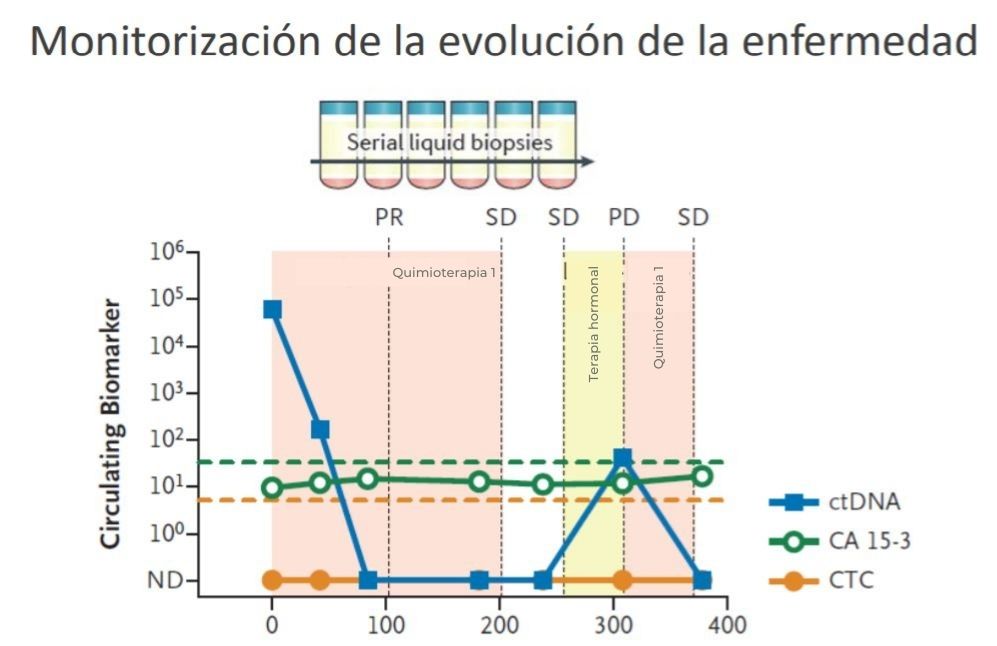
- En enfermedad metastásica puede ser muy útil para monitorizarla. Analizando el ADN tumoral en pacientes que empiezan un tratamiento como es la quimioterapia se ha visto que, si responde al tratamiento, los niveles se mantienen muy bajos. Si el tratamiento dejase de funcionar, volvería a subir esta cantidad y si se cambia a un tratamiento nuevo que sí funciona, volvería a bajar, tal y como vemos en la línea azul de la Gráfica 2 de abajo. Sin embargo, los marcadores que se reflejan en la gráfica con la línea verde, no son tan sensibles y su evolución no permite conocer si la enfermedad mejora o no. Además, en esta etapa permitiría conocer la agresividad de la enfermedad: a mayor cantidad de ADN tumoral que se detecte en la sangre el pronóstico será peor.
Gráfica 2. Monitorización de la evolución de la enfermedad. Dawson SJ aI. N Engl J Med. 2013 (adaptada por ONCONEWS by SOLTI).
Paradigma actual
Hace apenas dos años, las limitaciones de la biopsia líquida eran tales que se requerían estudios para determinar su efectividad.
Se consideraba entonces que la muestra tumoral en la sangre podía no ser verdaderamente representativa del ADN en el tumor real. Comparando con otras pruebas, se producían “falsos positivos”, es decir, se detectaba ADN canceroso cuando en realidad no se estaba desarrollando ningún cáncer. Sin embargo, se detectaban tumores en etapa temprana que no iban a crecer mucho o crecerían tan lentamente que en realidad nunca dañarían al paciente, con el consiguiente riesgo de sobretratamiento.
En la actualidad, la autoridad americana en materia de aprobación y vigilancia farmacológica, la FDA, ya ha aprobado varios ensayos en los que se incluye el uso de la biopsia líquida como diagnóstico complementario combinado con otras terapias específicas dirigidas del cáncer. Estas aprobaciones marcan un punto de inflexión para el uso generalizado de la biopsia líquida en la práctica clínica, y principalmente en pacientes con cáncer en estadio avanzado (3).
Tras los diferentes estudios retrospectivos que se requerían años atrás, la cada vez más creciente especificidad de la biopsia líquida permite, hoy en día, subministrar fármacos dirigidos a cada tumor en concreto. Próximamente, la biopsia líquida permitirá realizar una detección precoz de la enfermedad, antes de que aparezca el bulto, y de las recaídas. También permitirá predecir si un tratamiento acabará funcionando o no, y cambiarlo de manera temprana. Además, permitirá la monitorización de la enfermedad y ver qué va pasando durante el curso de manera más eficaz. Nos acercamos a una oncología más personalizada y de mayor precisión, dirigiendo tratamientos específicos a cada tumor.
El reto se encuentra ahora en el desarrollo de un conjunto (o panel como solemos llamarlo) de biomarcadores (una mutación es un “biomarcador”) para analizar cuantos más mejor en una sola muestra del paciente . Para ello, se requieren herramientas bioinformáticas sofisticadas como programas de aprendizaje automático, que permitirán contribuir significativamente al manejo no invasivo de pacientes individuales con cáncer. (1)
Referencias
(1) Keller, L., Belloum, Y., Wikman, H., & Pantel, K. (2021). Clinical relevance of blood-based ctDNA analysis: mutation detection and beyond. British Journal of Cancer, 124(2), 345–358. https://doi.org/10.1038/s41416-020-01047-5
(2) NCI Dictionary of Cancer Terms. (s. f.). National Cancer Institute. Recuperado 12 de mayo de 2021, de https://www.cancer.gov/publications/dictionaries/cancer-terms/def/liquid-biopsy
(3) Ignatiadis, M., Sledge, G. W., & Jeffrey, S. S. (2021). Liquid biopsy enters the clinic - implementation issues and future challenges. Nature reviews. Clinical Oncology, 18(5), 297–312. https://doi.org/10.1038/s41571-020-00457-x
(4) Ponencia impartida por la Dra. Olga Martínez (Hospital Clínic de Barcelona) en el Taller de Formación para Pacientes con cáncer de mama del 24 de marzo de 2021. Biopsia líquida en cáncer de mama.
En colaboración con:
 Irene Fernández
Irene Fernández